Az anyagcsere az a folyamat, amely során a bevitt tápanyagokat a szervezet
lebontja, feldolgozza és eljuttatja a rendeltetési helyükre.
Első lépés az
emésztés, melynek során a táplálékot a gyomorban ás a belekben fokozatosan
kisebb, szállítható energiahordozó egységekké kell alakítani, amelyek bekerülnek
a véráramba. Ezek a lebontott összetevők a glükóz, a zsírsavak és az
aminosavak, de ezek önmagukban nem energiaszolgáltató egységek, hanem könnyen
szállítható köztes termékek. Kétféle sors vár rájuk: vagy metabolizálódnak,
hogy részt vegyenek az energia termelésben, vagy tárolásra kerülnek a jövőbeni
felhasználás érdekében.
Az a glükóz, amit nem használunk fel azonnal, glükogénné alakul, amely
elsősorban az izmokban és a májban raktározódik. [1] A zsírsavak, amelyeket nem használunk
fel azonnal, a zsírsejtekbe kerülnek, ahol trigliceridekké alakulnak és ebben a
formában tárolódnak. [2] Az aminosavak nagy része az
izmok és a szervek fenntartásához használódik, de nincs tartalékraktáruk szűk
napokra. Amit nem használunk fel azonnal, bekerülnek a metabolikus
folyamatokba. A köztes termékek
akkor metabolizálódhatnak használható energiatermelő egységekké, amikor
eljutnak a célállomásukat jelentő szövetekhez és szervekhez. A második lépés
tehát a köztes anyagcsere, melynek során a köztes termékekből bonyolult
folyamatok során energia termelődik. Az energiahordozó egység az összes földi
élőlény esetében az adenozin-trifoszfát, röviden ATP. [3]
A köztes anyagcsere folyamata biztosítja, hogy a köztes termékekből
származó energia ne egyből, egy durva löketben szabaduljon fel, (értsd,
alakuljon át egyik formájából a másikba), hanem elosztva sok trillió ATP
molekulába, ahonnan ellenőrzött módon használható fel. [4] Az ATP
tulajdonképen egy molekuláris nagyságrendű újratölthető akkumulátor. Az energia
a trifoszfát rész kémiai kötéseiben tárolódik. A köztes termékek
anyagcseréjének célja, hogy átadja azt az energiát, amellyel az
adenozin-difoszfát, röviden ADP molekulához egy harmadik foszfátmolekula
kötődik és így ATP jön létre. Az energia abban a kémiai kötésben kerül
eltárolásra, amelyik a harmadik foszfátcsoportot rögzíti a másodikhoz. Ha a
folyamat fordítva zajlik le, a foszfátcsoportok szétválnak és a kötés energiája
felszabadul. A folyamat újra és újra megismétlődik a szervezetünket felépítő 37
billió sejt mindenikében. [5]
A sejtekben szüntelenül zajlanak a kémiai reakciók ezrei, amelyek a
sejt és az egész test fenntartásához és egészségéhez szükségesek. Ezek a kémiai
reakciók gyakran láncokká vagy útvonalakká kapcsolódnak össze. A sejten belüli
kémiai reakciók összességét sejtanyagcserének
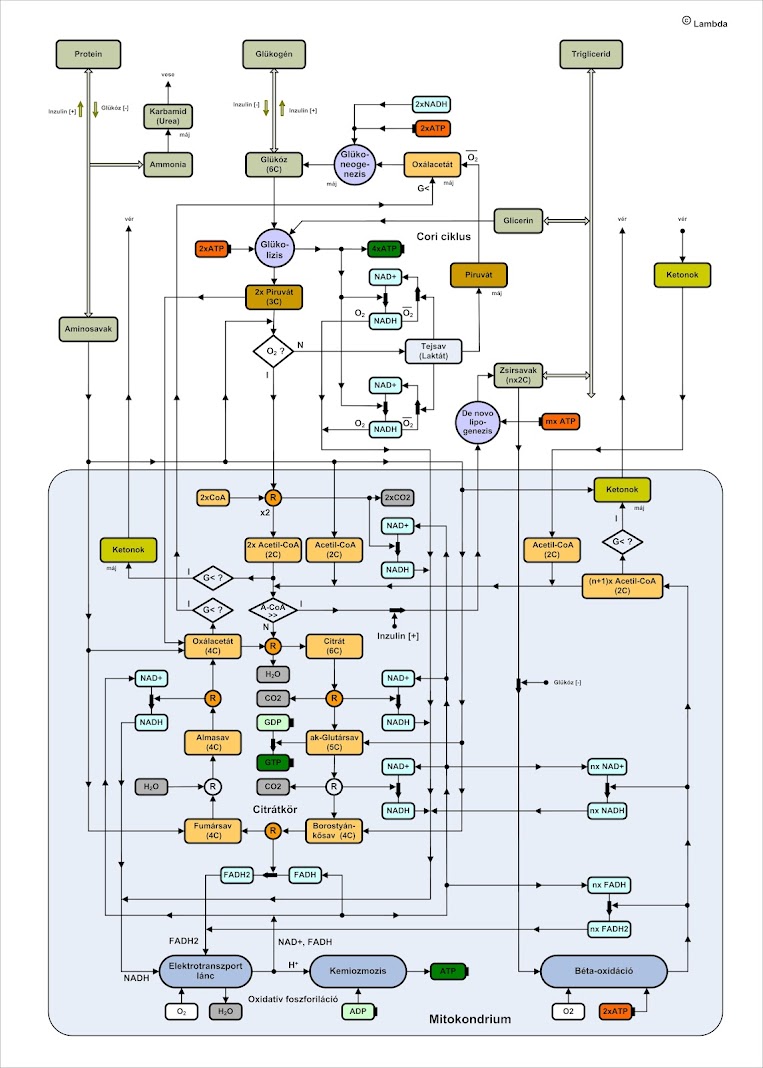
nevezzük. A mellékelt képen a legfontosabb anyagcsere-útvonalak folyamatábrája
látható egy olyan eukarióta sejtben, mint amilyenek az emberi testet is
alkotják. Az anyagcsere-útvonalakat alkotó kémiai reakciók nem automatikus,
irányítatlan folyamatok. Az útvonal minden egyes lépését enzimeknek nevezett fehérjék
segítik elő, azaz katalizálják.
A köztes tápanyagok metabolizmusa eltérő módon kezdődik, de az utak
összefutnak az acetil-koenzim-A, röviden acetil-CoA nevű molekulánál. A képződő
ATP mennyisége is különböző. Nézzük sorra a folyamatokat, a folyamatábra
alapján.
A szénhidrátok anyagcseréje a legegyszerűbb. A bélfalon át a vérkeringésbe
jutó végső lebomlási termék túlnyomó része glükóz. Miután a glükóz bekerül egy
sejtbe, vagy elraktározódik (glükogén), vagy metabolizálódik. Ennek első
szakasza a glükolízis, amelyben egy glükózmolekula két piruvát nevű vegyületre
(piroszőlősavra) hasad. A glükolízis
során minden glükózmolekula lebontása két ATP-be kerül, de négy ATP-t termel,
tehát a nettó bevétel két ATP molekula és közben elektronok felvétele révén két
NAD+ molekula két NADH molekulává alakul.
[6] A NADH
molekulának fontos szerepe van a mitokondriumban történő aerob ATP-t generáló
folyamatokban. A glükolízis azonban anaerob folyamat, vagyis nem kell hozzá
oxigén és a sejt citoplazmájában történik. A továbbiakban viszont az oxigén
határozza meg, hogy milyen irányt vesz a folyamat. Oxigén nélkül a piruvátból
laktát (tejsav) képződik, és visszakonvertálja a NADH-t NAD+-á, hogy
ellássa vele a glükolízist.
Bizonyos esetekben négy ATP és két NADH áráért a piruvát ismét glükózzá
alakítható a májban és a vesében. [7] A folyamat neve glükoneogenezis. Legfőbb
forrása a tejsav, amely alacsony oxigénszint mellett keletkezik az izmokban
piruvátból. A tejsav a vérkeringéssel a májba kerül, ahol visszaalakul
piruváttá. [!] A
következő lépésben a piruvát oxálacetáttá alakul. Utóbbi a glükoneogenezis
során glükózzá konvertálódik, majd a vér visszaviszi az izmokba, ahol a
glükolízis nyersanyaga lesz. A ciklikus folyamat neve Cori ciklus vagy
tejsavciklus. A máj éhezés közben csak akkor tudja fenntartani a
vércukorszintet, ha elég piruvát áll a rendelkezésére. Miután a piruvátból
acetil-CoA képződik, már nem alakítható vissza ezen az úton. Oxigén jelenlétében viszont minden piruvátból
acetil-CoA lesz, amely bejut a mitokondriumokba és belép az un. citrátkörbe
(Szent György-Krebs ciklus) amelyben NADH és FADH2 molekulák termelődnek,
melyek az ATP szintézisét táplálják. Mivel nem képződik több tejsav (mivel a
piruvát felhasználódott), a keverékhez hozzáadhatjuk a glükolízisben
keletkezett NADH-t is.
Az aerob (oxidatív) energiatermelés három kulcsfontosságú folyamatára a
mitokondriumokban kerül sor. [8]
Az
egyik a citrátkör majd az azt követő oxidatív foszforiláció, melyekben közös
úton történik a glükóz, zsírsavak és aminosavak lebomlásából származó
acetil-CoA átalakítása ATP-vé. A harmadik a béta-oxidáció, amelyben a zsírsavak
acetil-CoA-vá alakulnak.
A citrátkör a
természet egyik legjelentősebb találmánya. A legtöbb szén alapú égésfajtánál a
szén oxidációja (égése) szolgáltatja az energiát. Ez a folyamat azonban
szabályozatlan és az egyszerre keletkező nagy mennyiségű hő fatális lenne az
élőlények számára. A szerves molekulák bomlásakor viszont a felszabaduló
energiát azok a kémiai kötések tárolják, amelyek a sejteket összetartó
szénláncokban találhatók. A citrátkör ellenőrzött körülményei között a
szénatomok közötti kötések úgy bomlanak fel, hogy a felszabaduló energia
biztonságosan adagolódjon az oxidatív foszforiláció számára. A citrátkör az acetil-CoA-val kezdődik, már ha
egy körnek van kezdete. A molekula két szénatomot tartalmazó acetilcsoportja
reakcióba lép a négy szénatomos oxálacetáttal, hogy hat szénatomos citromsav
(citrát) jöjjön létre. Az ezt követő lépésekben két szénatom kiválik a
citrátból és oxigén jelenlétében két CO2 molekula képződik, és a végén ismét
létrejön az oxálacetát, amely képes rá, hogy egy újabb acetil-CoA-val
újrakezdje a ciklust. [9] A
folyamat oxidatív lépései során felszabaduló energia nagyenergiájú elektronok
formájában a NAD+-hoz jut és NADH képződik belőlük. A citrátkörben minden
acetil-CoA-ból három NADH és egy FADH2 molekula képződik, majd átviszik az
elektronrakományukat az oxidatív foszforiláció folyamatába. Ezek a molekulák
két olyan elektront hordoznak, amelyet átadhatnak. Ez azért fontos, mert ha egy
sejt protonok és elektronok mozgatásával elektromos gradienst
(feszültségkülönbséget) tud előidézni, akkor energiát tud generálni. A
citromsavciklust minden esetben oxidatív foszforiláció követi.
Az oxidatív
foszforiláció, vagyis oxigén felvétele annak érdekében, hogy az ADP
foszforilálódjon (felvegyen egy foszfátcsoportot), a belső mitokondriális
membrán redőiben zajlik, öt nagy fehérjekomplexum közreműködésével. Az elsőnél a NADH, a másodiknál a FADH2
szabadul meg egy-egy elektronjától és oxigénnel visszaoxidálódnak NAD+-á, illetve
FADH-vá, miközben víz képződik. A leadott elektronok un. elektrontranszport -láncon
(molekuláris átvitelen) keresztül jutnak el a negyedik komplexumhoz, miközben az
első, harmadik és negyedik komplexum protonokat (H+) szivattyúz ki a mátrixból
a belső membránon át a membránok közötti térbe. A membránok közötti térben levő
pozitív töltésű protonok és a mátrixban tárolt negatív töltésű elektronok
közötti elektromos gradienst az ötödik fehérje-komplex az un. ATP-szintáz használja
ki. Amikor elég nagy a feszültségkülönbség, a membránok közötti térből protonok
áramlanak ki az ATP-szintázon keresztül a mátrixba és elindítják azt a reakciót,
amelyben foszfátcsoport kapcsolódik az ADP-hez és ATP-vé alakul. Egy menet
alatt három ATP keletkezik. A folyamatot tápláló minden NADH két és fél, minden
FADH2 egy és fél ATP-t generál. Így
konvertálódik kalóriákká az ételekben tárolt energia. A citrátkörrel és az oxidatív foszforilációval
kapcsolatban összesen négyen kaptak kémiai Nobel díjat 1978 és 1997 között.
Számoljunk. Egyetlen mitokondrium belső membránján akár tízezer
ATP-szintáz is helyet kaphat. Egy sejt több ezer mitokondriumot is
tartalmazhat. Szervezetünkben mintegy 37 billió sejt található. Így tudunk
minden egyes nap a testünkkel megegyező tömegű ATP-t szintetizálni. Még
számoljunk. Szervezetünk két lépcsőben von ki energiát a glükózból. Az első a glükolízis,
amelyben két ATP keletkezik. Ez gyorsan megy végbe és ez történik a rövid ideig
tartó, intenzív erőfeszítéseknél. A második lépés az oxidatív foszforiláció,
amelyben további 28 ATP termelődik. Tehát oxigén jelenlétében összesen 30 ATP
képződik, míg oxigén nélkül csak 2, vagyis 15-ször kevesebb.
Most lássuk a zsírok anyagcseréjét. A zsírsejtekben a szervezet
alacsony energiaszintje esetén aktiválódik az un. hormonérzékeny lipáz enzim,
amely a trigliceridekből felszabadítja a zsírsavakat. A szabad zsírsavak
bekerülnek a vérkeringésbe, ahol az albumin nevű fehérje lesz a hordozójuk és eljuttatja
őket minden sejthez, amelynek üzemanyagként szüksége van rájuk. [10] Az
izomsejtekben nem képződnek trigliceridek, hanem a zsírsavak közvetlenül ATP
termelésre használódnak fel. A zsírsavak a mitokondriumokba kerülnek és a bétaoxidációjuk
révén részt vesznek az ATP generálásában. Ez több lépcsőben zajlik, és
mindenikben két szénatom hasad le a zsírsavláncról, miközben egy NADH, egy
FADH2 és egy acetil-CoA képződik. Az acetil-CoA belép a citrátkörbe (lásd,
folyamatábra), ahol még további három NADH és egy FADH2 keletkezik. Az egész
folyamat bámulatosan hatékony, mivel csak két ATP molekulába kerül. Egy tipikus
(16 szénatomos) zsírsavmolekula energiájával, oxigén jelenlétében 106 molekula
ATP generálható. [11]
Végül vizsgáljuk meg a fehérjék metabolizmusát. Ezekből komplikáltabban jutunk energiához. Először
is, a proteineket felépítő aminosavak nem egyformák. [12] Másodszor, a proteinek, a
szénhidrátoktól és zsíroktól eltérően, a C, H és O mellett jelentős mennyiségű
nitrogént is tartalmaz. Míg az emberi szervezet gond nélkül képes az előbbiek
tárolására, a nitrogént el kell távolítsa. Az amino-csoportokból ammónia lesz,
amelyet a transzportmechanizmusok eljuttatnak a májba, és ott karbamiddá
alakul, majd visszakerül a vérbe. A vese kivonja a vérből a karbamidot, amely a
húgyutakon távozik a vizelettel. A lebontási módszerek a következő lépésekben már
különböznek. Az aminosavak vagy glükogenikus típusok, vagy ketogén típusok. Az
előbbiek esetén, az amino-csoport leválasztása után visszamaradó szénváz, eltérő
pontokon, de egyszerűen beléphet a citrátkörbe. Az utóbbiak viszont lebontásuk
előtt ketontestekké alakulnak.
A gond az, hogy nincs aminosav raktárunk szűk napokra. Amit nem használunk fel azonnal, arról a
szervezetünk leszedi az amino-csoportot, a maradék pedig bekerül a citrátkörbe,
ahol azonnal acetil-CoA lesz belőle, vagy ketontestekké alakul, és azokból lesz
acetil-CoA. De ha túl sok az acetil-CoA, akkor zsírsavakká alakul át (de novo
lipogenezis, a bétaoxidáció fordítottjának megfelelő folyamat) azok pedig a
zsírsejtekben kerülnek eltárolódásra. Ugyancsak felháborító, hogy a glükózzal
is ez történik, miután megtelnek a glükózraktárak. A felesleges glükóz lebomlik
piruváttá, ebből bizony acetil-CoA lesz, amely zsírsavvá alakul és zsírként
tárolódik. Szóval, az összes felesleges energia kizárólag zsír formájában kerül
raktározásra. A köztes anyagcsere és energiatárolás teljes folyamatát az
inzulin vezérli. Az inzulin kezeli azt a kapcsolót is, amely az üzemanyagot
hordozó köztes termékek tárolási és lebomlási üzemmódja között választ. A magas inzulinszint (pl. étkezés után)
serkenti az aminosavak beépülését az izmokba, valamint az acetil-CoA-ból
történő zsírsavszintézist. Alacsony vércukorszint mellett (pl. koplalás), az
inzulin szintje is csökken, ez átkapcsol lebomlási üzemmódba, és a glükogén
lebomlik, hogy több legyen a vérben a glükóz. [13]
Mint láthattuk, az az oxálacetát normálisan pótlódik a citrátkörben, de
piruvátból is létrejöhet. Elég elérhető oxálecetsavnak kell lennie, amely
reakcióba léphet a glükózból és zsírokból keletkezett acetil-CoA-val, különben
lelassul a citrátkör. Bizonyos mennyiségű piruvátnak tehát nem acetil-CoA-vá
kell konvertálódnia, hanem oxálecetsavvá, hogy fenntartható legyen a citrátkör.
Miközben az acetil-CoA nagy része zsírsavakból termelődik, a bétaoxidációjuk
akkor hatékony, ha elegendő glükóz van ahhoz, hogy megfelelő mennyiségű
oxálecetsav keletkezzen. A zsírsavak tehát hatékonyabban oxidálódnak cukor
jelenlétében!
Alapesetben (szinte) az összes acetil-CoA belép a citrátkörbe, hogy
ATP-t generáljon. De több olyan helyzet is előfordulhat, amikor az acetil-CoA
termelése nagyon megnő. Éhezéskor, alacsony szénhidráttartalmú étrendnél,
elhúzódó intenzív fizikai tevékenység mellett a glükogénraktárak kiürülnek. A
máj erre glükoneogenezissel reagál, hogy fenntartsa a vér glükózszintjét, és ehhez
minden elérhető oxálecetsavat felhasznál. Ám de, ha oxálecetsavból nincs elég,
akkor lelassul a citrátkör és felszaporodik az acetil-CoA. Ráadásul, ha kevés a
szénhidrát, a szervezet elsősorban a zsírsavakból nyer energiát, de a zsírsavak
bétaoxidációja során még több acetil-CoA termelődik. Nos, ez nem vezet
egzisztenciális krízishelyzethez, mert ilyen esetekben az acetil-CoA jelentős
hányada ketontestekké, röviden ketonokká alakul, a ketogenezisnek nevezett folyamatban.
A májban keletkezett ketonokat azután a vér elszállítja a szervekhez (izmok,
szív, agy), minden mitokondriummal rendelkező sejt fel tudja venni és
visszakonvertálni üzemanyagként használható acetil-CoA-vá. Minden
mitokondriummal rendelkező sejt hasznosítani tudja a ketonokat, amelyek
visszakonvertálódnak üzemanyagként használható acetil-CoA-vá. Amikor a
ketonokból nyerünk energiát, az ATP termelés lassabb. Koplaláskor fehérjéket is
bontunk le aminosavakra, amelyek belépnek a citrátkörbe, ahol vagy oxálecetsav
lesz belőlük, amely a glükoneogenezisbe kerül, vagy acetil-CoA keletkezik,
amelyből ketontestek lesznek. Ezért sajnos nem csak a hájunkból, hanem az izomtömegünkből
is veszítünk egy keveset. De hát valamit valamiért, nem igaz?
-----------------------------------------------------------------------------
Hivatkozások
[1] A glükogén olyan energiaraktár, amely
gyorsan elérhető, ha hirtelen sok glükózra van szükség. Valamit valamiért.
Gyorsan elérhető, de nem hatékony megoldás. Sok helyet foglal és 1g glükogén
előállításához 3g vízre van szükség. Az izomzat legfeljebb 400g, a máj pedig 100g
tárolásra képes, a vérben pedig max. 5g glükóz kering. Mivel 1g glükóz 4 kcal
energiát szolgáltat, a glükogénraktárunk kb. egynapi szükségletünket (2000
kcal) képes fedezni.
[2]
Egy átlagos felnőtt szervezetében 10-20kg zsír van. Mivel 1g zsír 9 kcal
energiát szolgáltat, következik, hogy szervezetünk 90-180 kcal energiát tárol
zsír formájában. Ez a mennyiség 70-90 napig tud életben tartani, evés nélkül!
[3] Az
ATP molekula két részből áll: adenozin (három gyűrű és nitrogén), valamint
három foszfátból felépülő trifoszfátból. A foszfátmolekula egy foszfor és négy
oxigénatomból áll és sok kémiai energia kell a molekulák egyesítéséhez. Az
anyagcsere végső célja, hogy biztosítsa azt az energiát, amellyel a két
foszfátcsoportot tartalmazó adenozin-difoszfáthoz (ADP) egy harmadik
foszfátmolekula kötődhet és adenozin- trifoszfát (ATP) jön létre.
[4] A
szénnek oxigén jelenlétében történő elégetése sok hőenergiát szabadít fel,
miközben melléktermékként szén-dioxid keletkezik. Ha a tápanyagok metabolizmusa
során, a szén alapú szerves köztes termékek „elégetése” során az energia
hasonlóan durva löketben szabadulna fel, szó szerint felforrna a vérünk.
[5]
Egy átlagos napon egy átlagember szervezete 50-75 kg ATP-t használ fel, úgy,
hogy közben 500-750 alkalommal újrahasznosítja. Ez kb. 8x10exp23 ATP molekula
tömegének felel meg.
[6] A
citrátkörben az elektronhordozók szerepét a NAD+/NADH és a FADH/FADH2
molekulapárok töltik be. Amikor a NAD+ vagy FADH reakcióba lép a vízzel, NADH,
illetve FADH2 képződik, és ezek a molekulák két olyan elektront hordoznak,
amelyet leadhatnak.
[7] A
máj egyik fontos feladata a vércukorszint fenntartása. Ha a vércukorszint
alacsony, például koplalásnál vagy intenzív testgyakorlásnál, akkor a máj glükoneogenezissel
visszaállítja a glükózszintet a normális tartományba.
[8] A
mitokondriumok a sejt energiatermelésének specializálódott központjai. Két
membránjuk van, mindkettő egy-egy vékony kettős zsírmolekulákból (lipidekből)
álló réteg, amelyek elválasztják egymástól a vizet tartalmazó rekeszeket. a
belső membrán belsejében (mátrix) egy nagy fehérjemolekulákból álló komplexum
található, amely a légzés energiáját felhasználva pozitív hidrogénionokat azaz
protonokat mozgat a belső membránon keresztül, protongradienst hozva létre, vagyis
a membrán egyik oldalán nagyobb a protonok koncentrációja, mint a másik
oldalon. A membrán általában nem átjárható a protonok számára, ezt csak úgy
tehetik meg, ha keresztülhaladnak egy speciális molekulán (ATP-szintáz), amely
molekuláris turbinaként működik. Ez valóban turbinaként forog a protonok
áthaladásakor és ennek eredményeként egy ATP molekulát hoz létre azáltal, hogy egy
ADP molekulához hozzáad egy harmadik foszfátmolekulát.
[9] Miután
létrejött a 6 szénatomos citrát molekula, a következő lépésben átalakul saját
izomerjévé (izocitrát), majd oxidálódik és létrejön az 5 szénatomos ak-glutársav
(alfa-ketoglutarát), miközben egy CO2 molekula képződik és felszabadul két
elektron, melyek egy NAD+ molekulát NADH-vá redukálnak. A továbbiakban
irreverzibilis oxidatív dekarboxilezés során szukcinil-CoA képződik meg egy
molekula CO2, valamint egy NAD+ molekula redukálódik NADH-vá. A szukcinil-CoA
hidrolízise során borostyánkősav (szukcinát) képződik. Ehhez kapcsolódik egy
másik reakció, a szubsztrátszintű foszforiláció melyben egy nagy energiájú
kötés alakul ki: egy GDP (guanozin-difoszfát) molekula foszforilálódik GTP-vé. Következő
lépésben a borostyánkősav oxidálódik és fumársav (fumarát) képződik, miközben
egy FAD molekula redukálódik és a keletkező FADH2 hidrogénjei redukálják az ubikinont
ubikinollá. Egy vízmolekula
felvételével a fumársavból almasav (malát) képződik. A ciklus utolsó eleme a
malát oxálacetáttá való átalakulása, miközben még egy NAD+ molekula
redukálódik. A citromsavciklus több enzimét negatív visszacsatolásként
szabályozza az ATP, ha nagy a sejt energiatöltete. Ezek az enzimek, melyek a
citromsavciklus első három lépését szabályozzák, gátlódnak, ha megnő az ATP
koncentrációja. Ez a szabályzás biztosítja, hogy a citromsavciklus ne oxidáljon
piruvátot és acetil-CoA-t, ha elegendő ATP van a sejtben. Több enzim negatívan
szabályozódik, mikor a redukáló ekvivalensek szintje magas a sejtben (magas
NADH/NAD+ arány).
[10] A
zsírok nem oldódnak vízben, ezért nem lehet olyan egyszerűen szállítani őket a
vérrel, mint a cukrokat és a hidrofil aminosavakat, hanem csak hordozókkal
transzportálhatók. A legtöbb esetben, a triglicerideket a bélfalon át és a
vérben is un. kilomikronok szállítják, és egyenesen az izmokhoz kerülhetnek
üzemanyagként, vagy a zsírsejtekben elraktározódik a tartalmuk. Az izom- és
zsírsejtek felszínén lipázok találhatók, amelyek felismerik a kilomikronokat és
lehetővé teszik, hogy dokkoljanak a sejtekhez. Ugyanezek a lipázok leszedik a
zsírsavakat a glicerinvázról és a sejten kívüli térben létrejött szabad
zsírsavakat a sejtek már fel tudják venni. A zsírsejtek belsejében a szabad
zsírsavak glicerinmolekulákkal ismét trigliceridekké egyesülnek, míg az
izomsejtekben a zsírsavak direkt ATP termelésre használódnak fel. A legtöbb
sejt viszont nem ismeri fel a kilomikronokat, ezért a zsírsavat sem képesek
kivonni belőlük. Ezek a sejtek csak a már kibocsájtott zsírsavakat tudják
felhasználni.
[11] Ilyen
tipikus zsírsav a palmitinsav, amely a növényekben és állatokban előforduló
leggyakoribb telített zsírsav. A molekula egyik végén van a karboxilcsoport (-COOH),
amely minden zsírsavban azonos. Utána következik a változó hosszúságú szénlánc.
Pl. a palmitinsavban 16, a laurinsavban 12, az oleinsavban 18 szénatom található,
és így tovább. A telített zsírsavakban a karboxilcsoport kivételével minden
szénatom mind a négy kötése egyszeres, tehát négy különböző atomhoz
kapcsolódnak. Ha a szénláncban egy kettős kötés található, akkor a zsírsav
egyszeresen telítetlen. Ha egynél több kettős kötés van, akkor többszörösen telítetlen.
[12] Aminosavakból
húszféle van, az atipikus aminosavakkal 22 féle, és mindeniket kicsit eltérő
stratégiával kell lebontani.
[13] Nyugalomban, amikor sok a felesleges ATP,
több ATP molekula átalakul ADP-vé és a leadott foszfátcsoport a kreatin
molekulával foszfokreatinná egyesül. Hirtelen aktivitáskor, mikor a sejtekben
azonnal elérhető ATP elhasználódott (2-4 másodperc), a sejtek a
foszfokreatinban tárolt foszfátcsoportokkal feltöltik az ADP-ket ATP-kké, amit
rögtön fel tudnak használni. Ez a rendszer 8-10 másodpercnyi fizikai aktivitáshoz
elegendő energiát biztosít. Már az azonnal elérhető ATP és a foszfokreatin
felhasználása közben ezerszeresére nő a glükolízis intenzitása a rendelkezésre
álló glükózból. Kb. 10 másodpercnek kell
eltelnie ahhoz, hogy a glükolízis által termelt ATP elérhető legyen. Az azonnal
elérhető glükóz sem tart ki sokáig (kb. 30 másodperc), ezért a szervezet a májban
és izmokban levő glükogénraktárakhoz fordul. A gond, hogy a glükolízis anaerob
folyamat és oxigén hiányában a piruvát tejsavvá alakul. Ez a folyamat
legfeljebb 90 másodpercig tartható fenn, ezután elindulnak az aerob folyamatok
oxigén jelenlétében.
Megjegyzések
Megjegyzés küldése
Írd meg a véleményed: